安全性评价图表
FDA的安全性评价审批
药物临床试验的安全性评价是FDA审批的重要依据,包括不良事件(AE)和严重不良事件(SAE)。AE是指在药物治疗过程中,患者出现的不良事件,而SAE则是指AE中严重的不良事件。在药物临床试验中,我们通常会对AE和SAE进行统计分析,以评价药物的安全性。
在FDA的审批中,对于安全性数据的table和figure,有一些特殊的要求。
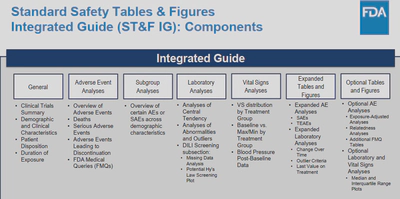
其中,AE的table的常见格式如下:
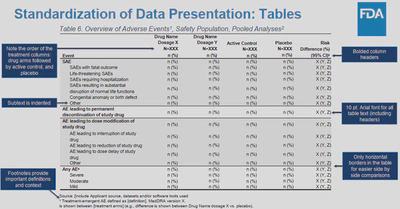
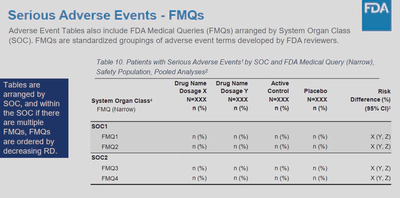
这个table的格式也适用于我们在科研文章期刊中的安全性数据的展示。对于SAE,包含了FDA medical queries,即FDA的医学查询。这些查询是FDA对于药物安全性的重点关注点,因此,我们在安全性数据的展示中,也需要对这些FMQs进行展示。
figure常见的format如下:
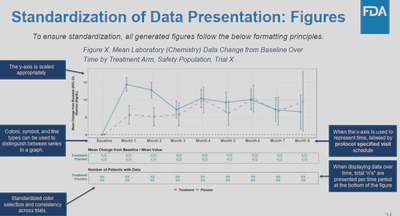
why standard safety tables & figures?
- 将安全信号评估标准化;
- 统一安全数据呈现和可视化(例如,颜色,表格布局);
- 遵循主要医学期刊使用的格式标准;
- 节省FDA reviewer时间。
why FDA medical queries?
- 类似的临床事件可能有不同的措辞术语;
- 不同的MedDRA PTs可以用于编码相同的医学概念;
- 不良事件可能以相关但不同的方式表现出来。